
Autorenfreundlich Bücher kaufen?!
Beschreibung
Bestandsaufnahme und Perspektiven
Details
| Verlag | Springer Berlin |
| Ersterscheinung | April 1991 |
| Maße | 24.2 cm x 17 cm |
| Gewicht | 205 Gramm |
| Format | Softcover |
| ISBN-13 | 9783540537984 |
| Seiten | 92 |
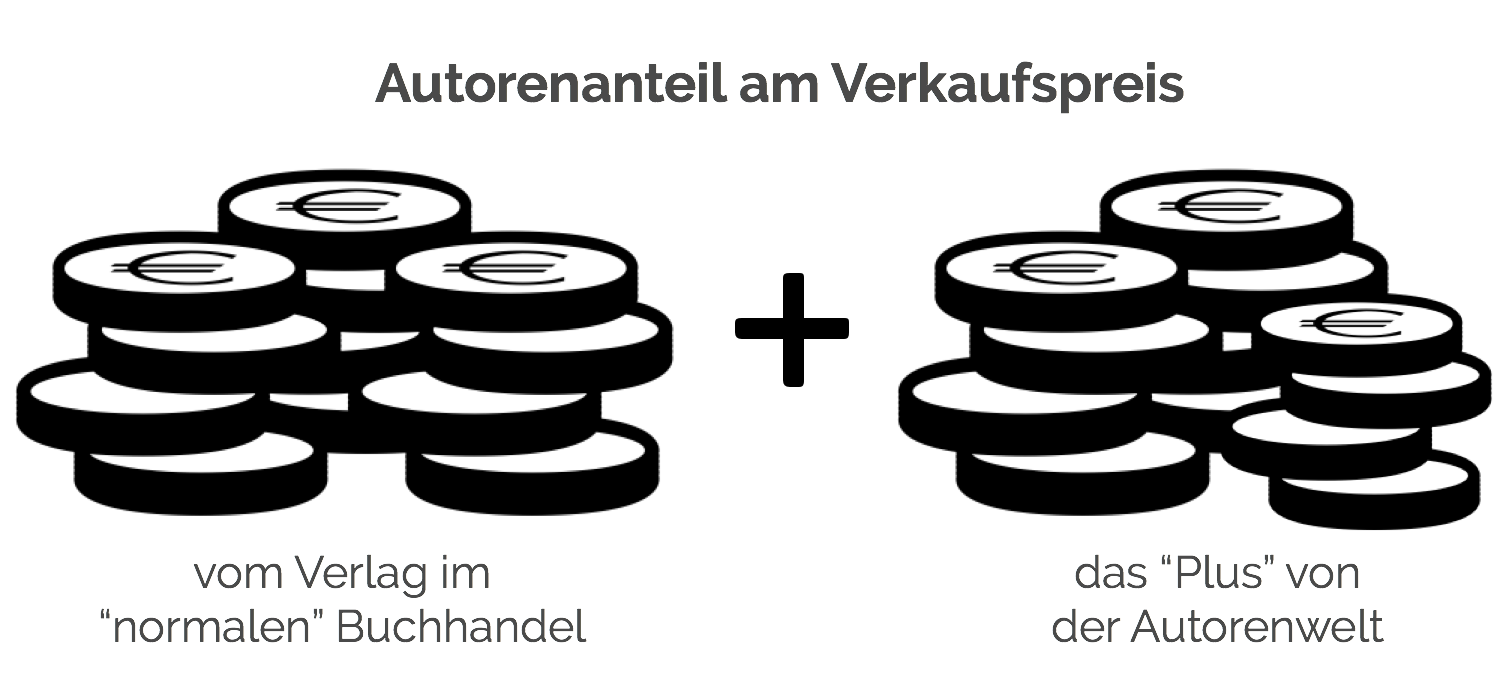
✍️ 🧑🦱 💚 Autor:innen verdienen bei uns doppelt. Dank euch haben sie so schon 393.427 € mehr verdient. → Mehr erfahren 💪 📚 🙏


| Verlag | Springer Berlin |
| Ersterscheinung | April 1991 |
| Maße | 24.2 cm x 17 cm |
| Gewicht | 205 Gramm |
| Format | Softcover |
| ISBN-13 | 9783540537984 |
| Seiten | 92 |